มาเข้าใจความหมายและสาเหตุของเชื้อดื้อยากันเถอะ
มาเข้าใจความหมายและสาเหตุของเชื้อดื้อยากันเถอะ
ดร.นิศานาถ เจริญลาภ
ดร.ไพบูลย์ วัฒนวิบูลย์
ศ.เกียรติคุณ ดร.ศกรณ์ มงคลสุข
ห้องปฏิบัติการวิจัยเทคโนโลยีชีวภาพ สถาบันวิจัยจุฬาภรณ์
ปัจจุบันนี้ มีการพูดถึงการดื้อยากันอย่างมาก แต่จะมีสักกี่คนที่เข้าใจสาเหตุ ที่มา ตลอดจนความหมายของคำว่า “ดื้อยา” ได้อย่างถูกต้อง จึงขออธิบายความหมายของคำว่า“ดื้อยา”และงานวิจัยทางด้านนี้ที่กำลังดำเนินการอยู่ที่สถาบันวิจัยจุฬาภรณ์มาเล่าสู่กันฟัง
การดื้อยาที่พูดถึงกัน ส่วนมากมีความหมายถึงการดื้อยาปฏิชีวนะ (Antibiotic Resistance) ซึ่งเป็นความสามารถของแบคทีเรียที่ทนต่อยาปฏิชีวนะชนิดใดชนิดหนึ่ง หรือมากกว่าหนึ่งชนิดก็ได้ ความสามารถนี้ไม่ใช่เรื่องใหม่ที่เพิ่งค้นพบ แต่เป็นความสามารถของแบคทีเรียที่สามารถปรับตัวให้อยู่รอดในสภาวะวิกฤตต่างๆ ได้ รวมทั้งสภาวะที่ต้องเผชิญกับยาปฏิชีวนะเช่นกัน การใช้ยาปฏิชีวนะมากเกินความจำเป็น หรือใช้อย่างไม่ถูกต้องจะทำให้แบคทีเรียมีวิวัฒนาการหรือปรับตัวให้ดื้อต่อยาปฏิชีวนะ ความสามารถดื้อต่อยาปฏิชีวนะของแบคทีเรียนี้จะไม่ใช่ปัญหาสำคัญถ้าหากอัตราการเกิดของแบคทีเรียดื้อยาที่มีความสามารถนี้ ไม่ได้เพิ่มสูงขึ้นอย่างรวดเร็วเช่นในปัจจุบัน อีกทั้งยังมีแบคทีเรียบางตัวที่มีความสามารถดื้อต่อยาปฏิชีวนะได้หลากหลายชนิด (Multidrug resistant bacteria, MDR) เรียกได้ว่า ไม่มียาปฏิชีวนะใดที่สามารถกำจัดแบคทีเรียชนิดนี้แล้ว ดังนั้น ถ้าเกิดการติดเชื้อจากแบคทีเรียนั้นๆ ก็จะไม่สามารถรักษาได้อีกต่อไป และผู้ป่วยที่ได้รับเชื้อดื้อยานั้นจะเสียชีวิตในที่สุด อุบัติการณ์เช่นนี้เองที่ทำให้ทั่วโลกตื่นตัว และหันมาให้ความสำคัญของการศึกษาการดื้อยา ซึ่งสถาบันวิจัยจุฬาภรณ์ได้เห็นปัญหานี้เช่นกัน และได้เริ่มศึกษาวิจัยเกี่ยวกับการดื้อยามาเป็นระยะเวลาหนึ่ง โดยคาดหวังว่าผลจากงานวิจัยนี้จะเป็นประโยชน์ต่อประชาชน อันเป็นการสนองต่อพระปณิธานของศาสตราจารย์ ดร. สมเด็จพระเจ้าน้องนางเธอเจ้าฟ้าจุฬาภรณวลัยลักษณ์ อัครราชกุมารี กรมพระศรีสวางควัฒน วรขัตติยราชนารี องค์ประธานสถาบันวิจัยจุฬาภรณ์ เพื่อให้งานวิจัยเกิดประโยชน์ต่อคนไทยและเพื่อให้คนไทยมีคุณภาพชีวิตที่ดีขึ้น
การที่จะสามารถแก้ไขปัญหาการดื้อยาได้นั้น จำเป็นต้องเข้าใจสาเหตุของปัญหาอย่างถ่องแท้เสียก่อนยาปฏิชีวนะมีกลไกการทำงานโดยการเข้าไปทำลายโมเลกุลเป้าหมายที่อยู่ในแบคทีเรีย ทำให้แบคทีเรียไม่สามารถเพิ่มจำนวนได้และตายในที่สุด กลไกการดื้อยาของเชื้อแบคทีเรียเกิดจาก 3 กลไก ดังแสดงในรูปที่ 1![]() ได้แก่ 1) แบคทีเรียมีความสามารถเปลี่ยนแปลงโมเลกุลเป้าหมาย (สีเขียว) ของตัวเองให้รอดพ้นจากการจับของยาปฏิชีวนะ (สีแดง) ดังนั้นยาปฏิชีวนะจึงไม่สามารถทำลายโมเลกุลเป้าหมายได้อีกต่อไป ส่วนมากมักเกิดจากการกลายพันธุ์ของแบคทีเรียที่ถูกเหนี่ยวนำจากการใช้ยาปฏิชีวนะที่ไม่เหมาะสม เช่น ความเข้มข้นยาปฏิชีวนะที่ต่ำเกินไป หรือระยะเวลาที่ใช้ยาปฏิชีวนะน้อยเกินไป ไม่ครบตามปริมาณที่กำหนด 2) แบคทีเรียสามารถผลิตเอนไซม์ที่ทำลายยาปฏิชีวนะให้หมดฤทธิ์ได้ (สีส้ม) 3) แบคทีเรียสามารถลดปริมาณยาปฏิชีวนะภายในเซลล์ โดยลดความสามารถของโปรตีนที่เยื่อหุ้มเซลล์เซลล์ทำให้นำเข้ายาปฏิชีวนะลดลง หรือผลิตโปรตีนขับยาปฏิชีวนะออกจากเซลล์ (efflux pump) ดังนั้นยาปฏิชีวนะจึงไม่สามารถฆ่าแบคทีเรียได้ โดยทั่วไปแบคทีเรียดื้อยามักมีความสามารถดังกล่าว อย่างน้อยหนึ่งกลไก ซึ่งเพียงพอที่จะทำให้เกิดการดื้อยาแล้ว
ได้แก่ 1) แบคทีเรียมีความสามารถเปลี่ยนแปลงโมเลกุลเป้าหมาย (สีเขียว) ของตัวเองให้รอดพ้นจากการจับของยาปฏิชีวนะ (สีแดง) ดังนั้นยาปฏิชีวนะจึงไม่สามารถทำลายโมเลกุลเป้าหมายได้อีกต่อไป ส่วนมากมักเกิดจากการกลายพันธุ์ของแบคทีเรียที่ถูกเหนี่ยวนำจากการใช้ยาปฏิชีวนะที่ไม่เหมาะสม เช่น ความเข้มข้นยาปฏิชีวนะที่ต่ำเกินไป หรือระยะเวลาที่ใช้ยาปฏิชีวนะน้อยเกินไป ไม่ครบตามปริมาณที่กำหนด 2) แบคทีเรียสามารถผลิตเอนไซม์ที่ทำลายยาปฏิชีวนะให้หมดฤทธิ์ได้ (สีส้ม) 3) แบคทีเรียสามารถลดปริมาณยาปฏิชีวนะภายในเซลล์ โดยลดความสามารถของโปรตีนที่เยื่อหุ้มเซลล์เซลล์ทำให้นำเข้ายาปฏิชีวนะลดลง หรือผลิตโปรตีนขับยาปฏิชีวนะออกจากเซลล์ (efflux pump) ดังนั้นยาปฏิชีวนะจึงไม่สามารถฆ่าแบคทีเรียได้ โดยทั่วไปแบคทีเรียดื้อยามักมีความสามารถดังกล่าว อย่างน้อยหนึ่งกลไก ซึ่งเพียงพอที่จะทำให้เกิดการดื้อยาแล้ว
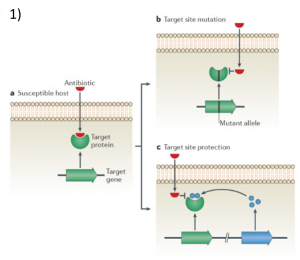
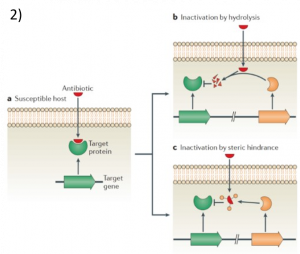
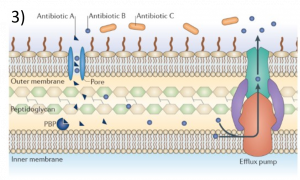
รูปที่ 1. 1) แบคทีเรียมีความสามารถในการเปลี่ยนแปลงโมเลกุลเป้าหมาย 2) แบคทีเรียเปลี่ยนแปลงยาปฏิชีวนะให้เสียสภาพ
3) แบคทีเรียลดปริมาณยาปฏิชีวนะภายในเซลล์ (Blair et al., 2015)
ทั้งนี้ ห้องปฏิบัติการวิจัยเทคโนโลยีชีวภาพ สถาบันวิจัยจุฬาภรณ์ โดย ศาสตราจารย์เกียรติคุณ ดร.ศกรณ์ มงคลสุข ดร.ไพบูลย์ วัฒนวิบูลย์ และดร.นิศานาถ เจริญลาภ ได้สนใจศึกษาโปรตีนขับยาปฏิชีวนะ (Efflux pump) ในเชื้อแบคทีเรียก่อโรคในคน คือ Stenotrophomonas maltophilia คณะผู้วิจัยโดย ดร.นิศานาถ เจริญลาภ ได้นำเสนอผลงานวิจัยนี้ในงานประชุมวิชาการกรมวิทยาศาสตร์การแพทย์ ครั้งที่ 25 และได้รับรางวัลชนะเลิศ ประเภทนำเสนอผลงานด้วยวาจา สาขา Medical Science Symposium เมื่อวันที่ 24 มีนาคม พ.ศ. 2560 บทสรุปของงานวิจัยโดยย่อมีดังนี้

เชื้อแบคทีเรีย Stenotrophomonas maltophilia จัดอยู่ในกลุ่มเชื้อฉวยโอกาสที่ก่อโรคติดเชื้อในโรงพยาบาล สามารถก่อโรคในทุกระบบของร่างกายโดยเฉพาะอย่างยิ่ง ระบบทางเดินหายใจ ทางเดินปัสสาวะ และการติดเชื้อในกระแสโลหิต ปัจจุบันนับว่าเป็นหนึ่งในสาเหตุสำคัญของการเสียชีวิตของผู้ป่วยจากโรคติดเชื้อในโรงพยาบาล ปัญหาสำคัญของการติดเชื้อ S. maltophilia เกิดจากการดื้อต่อยาปฏิชีวนะหลายชนิด (MDR) จากการศึกษาจีโนม ของเชื้อชนิดนี้พบว่ามียีนส์ที่เกี่ยวของกับการดื้อยาอยู่เป็นจำนวนมาก ไม่ว่าจะเป็นเอนไซม์ที่ทำให้ยาหมดฤทธิ์ เสียสภาพ หรือ โปรตีนขับยาชนิดต่างๆออกจากเซลล์![]()
ห้องปฏิบัติการวิจัยเทคโนโลยีชีวภาพ ได้ศึกษาวิจัยเพื่อหาสาเหตุการดื้อต่อยาปฏิชีวนะหลายชนิดของเชื้อ S. maltophilia โดยมุ่งเน้นการดื้อยาที่เกิดจากโปรตีนขับยา วัตถุประสงค์หลักของงานวิจัยนี้เพื่อการศึกษาโปรตีนที่เป็นเป้าหมายของยา คณะผู้วิจัยสามารถแยกยีน mfsA ที่สร้างโปรตีนขับยา MfsA ซึ่งเป็นโปรตีนที่ชั้นเยื่อหุ้มเซลล์ของแบคทีเรีย (membrane protein) ที่สามารถขนส่งสารชนิดต่างๆ ผ่านเยื่อหุ้มเซลล์โดยใช้พลังงานจากโปรตอน (proton gradient)![]()
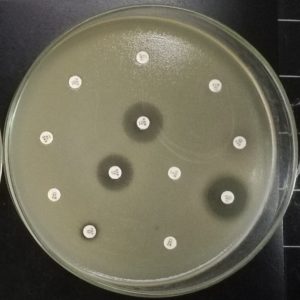
ในการวิจัยเมื่อสร้างแบคทีเรียกลายพันธุ์ที่ไม่มียีน mfsA (DmfsA) ทำให้แบคทีเรียมีความไว (susceptibility) ต่อยาปฏิชีวนะหลายชนิดมากขึ้น รวมถึงมีความไวต่อยาในกลุ่มฟลูออโรควิโนโลน (fluoroquinolones)![]() ซึ่งเป็นยาชนิดหนึ่งในกลุ่มยาที่มักใช้ในการรักษาการติดเชื้อจาก S. maltophilia และเมื่อเพิ่มการแสดงออกของยีน mfsA โดยใช้พลาสมิด พบว่าทำให้เชื้อดื้อต่อยาปฏิชีวนะฟลูออโรควิโนโลน (fluoroquinolones) เพิ่มมากขึ้นหลายเท่า
ซึ่งเป็นยาชนิดหนึ่งในกลุ่มยาที่มักใช้ในการรักษาการติดเชื้อจาก S. maltophilia และเมื่อเพิ่มการแสดงออกของยีน mfsA โดยใช้พลาสมิด พบว่าทำให้เชื้อดื้อต่อยาปฏิชีวนะฟลูออโรควิโนโลน (fluoroquinolones) เพิ่มมากขึ้นหลายเท่า
จากการศึกษาทำให้ค้นพบลักษณะที่น่าสนใจของยีน mfsA โดยพบว่า การแสดงออก (expression) ของยีน mfsA จะเพิ่มขึ้นอย่างมากเมื่อเชื้อสัมผัสกับอนุมูลอิสระออกซิเจนชนิดซุปเปอร์ออกไซด์แอนไอออน (superoxide anion) เนื่องจากยีน mfsA ถูกควบคุมโดยโปรตีนควบคุม (transcriptional regulator) ที่ชื่อว่า SoxR ![]() รูปที่ 2 แสดงให้เห็นว่าเมื่อ S. maltophilia สัมผัสกับ ซุปเปอร์ออกไซด์แอนไอออน ที่สร้างโดยเซลล์เม็ดเลือดขาวในกลุ่มแมคโครฟาจ (macrophage) ในระบบภูมิคุ้มกันชนิดทั่วไป (innate immunity) ทำให้โปรตีนควบคุม SoxR กระตุ้นการสร้างโปรตีนขับยา MfsA เพิ่มมากขึ้น อันเป็นสาเหตุให้เชื้อดื้อต่อยาปฏิชีวนะกลุ่มฟลูออโรควิโนโลน (fluoroquinolones) มากขึ้น การค้นพบนี้มีความน่าสนใจเนื่องจากยากำจัดวัชพืชพาราควอท ก็จัดอยู่ในประเภทสารที่ทำให้เกิด ซุปเปอร์ออกไซด์แอนไอออน ในเซลล์ได้เช่นกัน เมื่อวิเคราะห์ข้อมูลจากฐานข้อมูลทางจีโนม The National Center for Biotechnology Information (NCBI) พบว่าเชื้อ S. maltophilia ทุกสายพันธุ์มียีน mfsA ดังนั้น โปรตีนขับยา MfsA จึงเหมาะสมที่จะเป็นเป้าหมาย ตามสมมุติฐานที่ตั้งไว้คือ ถ้าสามารถคัดเลือกสารที่สามารถยับยั้งการทำงานของโปรตีนขับยา MfsA ได้ เมื่อนำสารดังกล่าวมาใช้จะทำให้เชื้อแบคทีเรียกลับมาไวต่อยาปฏิชีวนะฟลูออโรควิโนโลน (fluoroquinolones) ได้เช่นเดิม ดังนั้น องค์ความรู้ที่ได้จากงานวิจัยนี้นับเป็นประโยชน์อย่างยิ่งในการพัฒนายาตัวใหม่สำหรับรักษาโรคติดเชื้อได้ในอนาคต
รูปที่ 2 แสดงให้เห็นว่าเมื่อ S. maltophilia สัมผัสกับ ซุปเปอร์ออกไซด์แอนไอออน ที่สร้างโดยเซลล์เม็ดเลือดขาวในกลุ่มแมคโครฟาจ (macrophage) ในระบบภูมิคุ้มกันชนิดทั่วไป (innate immunity) ทำให้โปรตีนควบคุม SoxR กระตุ้นการสร้างโปรตีนขับยา MfsA เพิ่มมากขึ้น อันเป็นสาเหตุให้เชื้อดื้อต่อยาปฏิชีวนะกลุ่มฟลูออโรควิโนโลน (fluoroquinolones) มากขึ้น การค้นพบนี้มีความน่าสนใจเนื่องจากยากำจัดวัชพืชพาราควอท ก็จัดอยู่ในประเภทสารที่ทำให้เกิด ซุปเปอร์ออกไซด์แอนไอออน ในเซลล์ได้เช่นกัน เมื่อวิเคราะห์ข้อมูลจากฐานข้อมูลทางจีโนม The National Center for Biotechnology Information (NCBI) พบว่าเชื้อ S. maltophilia ทุกสายพันธุ์มียีน mfsA ดังนั้น โปรตีนขับยา MfsA จึงเหมาะสมที่จะเป็นเป้าหมาย ตามสมมุติฐานที่ตั้งไว้คือ ถ้าสามารถคัดเลือกสารที่สามารถยับยั้งการทำงานของโปรตีนขับยา MfsA ได้ เมื่อนำสารดังกล่าวมาใช้จะทำให้เชื้อแบคทีเรียกลับมาไวต่อยาปฏิชีวนะฟลูออโรควิโนโลน (fluoroquinolones) ได้เช่นเดิม ดังนั้น องค์ความรู้ที่ได้จากงานวิจัยนี้นับเป็นประโยชน์อย่างยิ่งในการพัฒนายาตัวใหม่สำหรับรักษาโรคติดเชื้อได้ในอนาคต
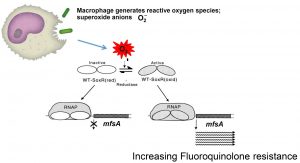
รูปที่ 2 โปรตีนควบคุม SoxR ควบคุมการแสดงออกของยีนที่สร้างโปรตีนขับยา MfsA ในสภาวะที่ถูกกระตุ้นด้วยสารอนุมูลอิสระชนิด superoxide anion ซึ่งสร้างโดยเซลล์ภูมิคุ้มกัน Macrophage ยีนโปรตีนขับยาจะเพิ่มมากขึ้น ส่งผลให้แบคทีเรียดื้อต่อยาปฏิชีวนะกลุ่ม fluoroquinolones มากขึ้น
References:
- Blair, J. M., M. A. Webber, A. J. Baylay, D. O. Ogbolu, and L. J. Piddock. 2015. Molecular mechanisms of antibiotic resistance. Nat Rev Microbiol 13:42-51.
- Crossman, L. C., V. C. Gould, J. M. Dow, G. S. Vernikos, A. Okazaki, M. Sebaihia, D. Saunders, C. Arrowsmith, T. Carver, N. Peters, E. Adlem, A. Kerhornou, A. Lord, L. Murphy, K. Seeger, R. Squares, S. Rutter, M. A. Quail, M. A. Rajandream, D. Harris, C. Churcher, S. D. Bentley, J. Parkhill, N. R. Thomson, and M. B. Avison. 2008. The complete genome, comparative and functional analysis of Stenotrophomonas maltophilia reveals an organism heavily shielded by drug resistance determinants. Genome Biol 9:R74.
- Dulyayangkul, P., N. Charoenlap, K. Srijaruskul, S. Mongkolsuk, and P. Vattanaviboon. 2016. Major facilitator superfamily MfsA contributes to multidrug resistance in emerging nosocomial pathogen Stenotrophomonas maltophilia. J Antimicrob Chemother 71:2990-1.
- Srijaruskul, K., N. Charoenlap, P. Namchaiw, S. Chattrakarn, S. Giengkam, S. Mongkolsuk, and P. Vattanaviboon. 2015. Regulation by SoxR of mfsA, Which Encodes a Major Facilitator Protein Involved in Paraquat Resistance in Stenotrophomonas maltophilia. PLoS One 10:e0123699.

